云南师范大学附属怒江州民族中学 673200
摘要:化学是一门研究物质的组成、结构、性质的科学,物质性质的学习是高中的重点内容,在高考中也占很大比例,怎样使学生从学科思想的高度去深入学习物质的性质,以氯气的性质教学为例加以研究。
关键字:模型认知、类别、化合价
POE教学策略是一种以学生为主体,教师通过引导学生进行预测、观察、解释,最终使学生达成自主构建、完成概念转变的策略[1]。
元素及其化合物的种类众多,教材中选取了典型的代表物进行学习,如钠元素、铁元素、硅元素、氯元素、氮元素、硫元素等,在元素及其化合物的教学过程中,利用POE教学策略用理论指导学生去预测,然后对预测结果进行验证,若验证与预测相符,则预测正确,并得出结论,若验证与预测不相符,则预测错误,需要重新预测,直至验证与预测一致。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
任务一、氯气的化学性质
问题:从物质的分类和化合价两个视角预测氯气可能具有的化学性质?
1、预测:⑴从物质分类的角度来看,氯气属于非金属单质,学生最熟悉的非金属单质是氧气,根据学生所具备的知识,如镁条可以在氧气中燃烧,碳在点燃条件下可以和氧气等,预测氯气可能和金属单质或某些非金属单质反应。
⑵从原子结构的角度来看,氯的最外层有7个电子,容易得到一个电子,化合价由0价变到-1价较容易,预测氯气具有强氧化性,可以氧化一些具有还原性的物质。
2、实验验证:
实验1、金属钠在氯气中的燃烧
实验2、金属铜在氯气中的燃烧
实验3、金属铁在氯气中的燃烧
实验4、非金属单质氢气在氯气中的燃烧
3、结论:由以上实验发现,氯气这种非金属单质除了能和金属单质反应,还能和非金属单质氢气反应,在反应过程中,氯元素的化合价都降低,体现了预测中氯气的氧化性,并且在与变价金属铁、铜反应时,将他们氧化为较高价态,说明氯气具有强氧化性。进一步引导学生回忆氧化还原反应的相关知识,分析出氯气不仅可以氧化金属单质和非金属单质,还可以氧化其它具有还原性的一些物质,如Fe2+、I-等。
任务二、探究氯气与水的反应
环节一、探究氯水的成分
问题:根据科学史话--瑞典化学家舍勒偶然机会制出了一种黄绿色气体(实际上是氯气),通过多次实验发现,它可以溶于水,可以使有色的蔬菜、花等永久性变白。后来法国化学家贝托莱发现这种黄绿色气体的水溶液在日光照射下漂白性消失。预测氯水的成分?
1、预测氯水的成分:
⑴氯气和水没有发生反应,氯水的成分为氯气和水。
⑵氯气和水全部发生了反应 ,氯水的成分为新物质和水。
⑶氯气和水部分发生反应,氯水的成分为氯气、新物质和水。
2、实验验证
实验 | 现象 |
实验1、观察氯水的颜色 | 氯水有浅黄绿色 |
实验2、干燥的氯气与干燥的有色花瓣作用 | 干燥的氯气不能使干燥的有色花瓣褪色 |
实验3、湿润的氯气与有色花瓣作用 | 湿润的氯气可以使有色花瓣褪色 |
3、结论:根据实验2发现氯气本身没有漂白性,结合实验1和实验3发现,氯气和水部分发生了反应,预测3正确。
环节二、探究氯气与水反应的产物
问题:已知氯气与水发生反应起到漂白性的物质是次氯酸,Cl2+H2O→HClO+?,根据所学氧化还原知识预测还有其他产物吗?若有,产物可能是什么?
1、预测:根据所学氧化还原反应的基本知识分析,Cl2生成HClO的过程中,氯元素的化合价升高,若只有一种产物,不符合氧化还原反应的规则--化合价有升有降,所以必然有另一种化合价降低的产物,预测可能是生成了HCl,即氯气发生了歧化反应。
2、验证:采用数字化仪器氯离子传感器,发现氯水中确实存在Cl-
3、结论:氯气与水反应生成盐酸和次氯酸,并且反应不完全,Cl2+H2O⇌HClO+HCl 。
环节三、探究次氯酸光照分解产物
问题:氯气的水溶液在日光照射下漂白性消失,原因可能是什么呢?
1、预测:从类别的角度来说,次氯酸属于弱酸,具有酸的通性,从化合价的角度分析次氯酸中氯元素的化合价为+1价,属于中间价态,既有氧化性又有还原性。光照时没有加入其他物质,从类别的角度可能是由于次氯酸类似于碳酸,不稳定发生了分解,从氧化还原的角度来看,次氯酸可能发生了歧化反应,有可能生成盐酸和氧气。
2、实验验证:可以从基础实验的角度验证光照时有氧气生成,光照时用带火星木条检验,可以用pH计测定溶液的pH变化。也可以用数字化实验进行验证,光照时随着时间的变化氯水的pH,氯离子浓度,氧气的体积分数变化的角度进行验证,或者直接引导学生参考教材图片,如下图。
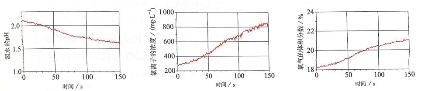
3、结论:次氯酸不稳定,光照时会分解,生成盐酸和氧气。
任务三、探究氯气与碱的反应
1、预测氯气与碱可以反应
由于氯气与水反应生成盐酸和次氯酸,而盐酸和次氯酸都可以和碱反应。
Cl2+H2O⇌HClO+HCl HClO+NaOH=NaClO+H2O HCl+NaOH=NaCl+H2O
对方程式进行叠加,分析出氯气可以和碱反应。
Cl2+2NaOH=NaCl+NaClO+H
2O
2、实验验证氯气可以和碱发生反应
分别向两个充满氯气的塑料瓶中分别滴加等量的水和氢氧化钠溶液,发现两个塑料瓶都会变憋,但滴加氢氧化钠的塑料瓶憋得程度更大。
3、结论:氯气可以和碱发生反应,并且反应程度比氯气与水反应的程度更大。
在氯气的教学中仅仅围绕着预测--验证--结论的策略展开,引导学生先根据物质类别和化合价两个视角去预测,符合学生的认知过程,利于学生接受,然后进行验证,从实验的角度或相关数据的角度对预测内容进行验证,最后再对结果进行总结,符合知识的生成过程,有利于培养学生形成学习元素化合物知识的思想模型。
[1]POE教学策略在高中化学实验教学中的实践研究 云南师范大学 甘诗霞 社会科学Ⅱ辑