1新疆全安药业股份有限公司(新疆甘草及制品研究重点试验室) 新疆维吾尔自治区巴音郭楞蒙古自治州库尔勒市, 841011; 2.塔里木大学生命与科学学院 新疆维吾尔自治区阿拉尔市 843300
摘要:目的:建立研究D101大孔树脂纯化甘草酸的工艺。方法:从单因素(样品溶解乙醇浓度、上样浓度、上样体积、上样量、吸附时间、解析液乙醇浓度、乙醇用量、解吸附时间)方面考察纯化甘草酸的树脂、最佳条件。结果:选用D101大孔吸附树脂作为填充材料分离纯化甘草酸,用20 %乙醇溶解粗品,上样浓度2 mg·ml-1,上样体积1 BV,上样液pH=5,解吸液为70 %乙醇,解吸液用量为5 BV,吸附时间为1.5 h,解吸附时间为2h。通过得到的最佳单因素,进行工艺组合确定最佳工艺下甘草酸转化率和含量。结论:在以上条件下甘草酸的吸附率为69.03 %,解吸率为91.76 %,转化率为79.21 %,纯度为36.45 %。
关键词:大孔树脂;甘草酸;纯化;工艺;
中图分类号:O657.99 文献标识码:A
甘草的主要成分甘草酸可以消炎解毒、防治病毒性肝炎和高血脂症,此外对癌症、艾滋病也有显著疗效。甘草酸在医药、烟草、酿造、食品添加剂(低热值甜味剂)、化妆品等方面广泛应用[1]。对于甘草酸的精制方法,主要包括超滤法、溶剂法(结晶法)、树脂法、聚酰胺法等,工业生产中主要应用溶剂法,但树脂法中的大孔树脂吸附法精制效果好,其纯化原理是借助大孔树脂与物质的范德华力或氢键的作用达到吸附的目的,由树脂本身的孔型结构决定筛选种类最终达到分离纯化的目的[2-3]。传统的甘草酸的生产工艺存在着诸多的不足,造成甘草利用率不高的同时污染环境。
1 材料与仪器
1.1 实验材料
甘草酸标准品购买于上海源叶生物科技有限公司(含量> 98%)。
甘草制品由新疆全安药业股份有限公司提供(批号:20180811)。
大孔树脂(D101):天津市光复精细化工研究所
试剂:无水乙醇(分析纯)、乙腈(色谱纯)、甲酸(色谱纯)
1.2 实验仪器
万分之一电子分析天平,Waters高效液相色谱e2695-2489,Inertsustain C18 色谱柱 (4.6 × 250 mm, 5 μm, Shimadzu公司)。
2 试验方法
2.1大孔树脂预处理:用蒸馏水冲洗大孔树脂直至流出液不呈浑浊状态,再用2倍量95%乙醇冲洗大孔树脂,2倍量95%乙醇浸泡24 h后,用蒸馏水冲洗至无乙醇味。
2.2 供试样品溶液配制:秤取样品粉末5.0000 g,用100 ml 20 %乙醇溶解并转移至1 L容量瓶中,用20%乙醇定容至刻度线,配制成5 mg·ml-1的供试样品溶液。
2.3 单因素试验设计
2.3.1动态吸附:
分别量取经预处理后D101大孔树脂50ml,依据不同的单因素条件设置(如表1),转移至吸附柱中,控制其流速流出,即可得吸附残液。
表1 动态吸附单因素变量设置
上样体积/BV | 解吸液体积/BV | 上样/pH | 上样浓度/ mg·ml-1 | 上样液乙醇液浓/% | 吸附时间/h | 解吸时间/h |
1 | 1 | 5 | 2 | 20 | 30 | 0.5 |
2 | 2 | 6 | 3 | 30 | 40 | 1 |
3 | 3 | 7 | 4 | 40 | 50 | 1.5 |
4 | 4 | 8 | 5 | 50 | 60 | 2 |
5 | 5 | 9 | 6 | 60 | 70 | 2.5 |
(2)再根据各单因素的条件设置加入解吸液,控制其流速流出,即可得解吸液。
3. 讨论与结果
3.1 高效液相色谱法测定
精确称取4 ℃下保存的甘草酸对照品,用50 %乙醇溶液溶解并定容。以50 %乙醇为空白,参考不同文献[4-7],在250 nm、252 nm、254 nm、256 nm、265 nm波长下测定其吸光度,发现甘草酸对照品在252 nm下有最大吸收,于是选定252 nm作检测甘草酸的最大吸收波长。
3.1.1标准曲线的绘制
精确称取4℃下保存的甘草酸对照品0.0100 g,用50 %乙醇溶液溶解并定容至10mL。分别精密吸取0.25、0.50、0.75、1.00、1.25、1.50 mL此溶液于25 mL容量瓶中,再用50 %乙醇定容至25mL。色谱条件为:Inertsustain C18 色谱柱 (4.6 × 250 mm, 5μm),以乙腈:0.05 %甲酸水为流动相,柱温为30 ℃,检测波长为252 nm,流速为1.0 mL·min-1。用0.45 μm的微孔滤膜过滤,分别进样10 μL,参照2020年药典的测定方法进行检测。以甘草酸对照品的浓度为横坐标,峰面积为纵坐标进行回归分析,得到浓度与峰面积之间的回归方程并绘制标准曲线,如图1所示。
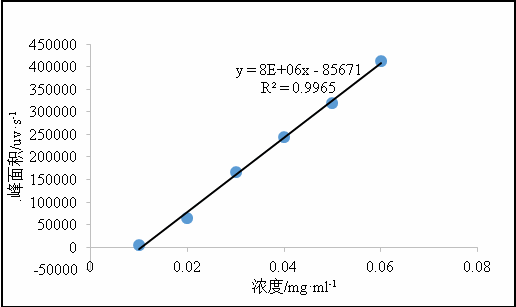
图1 252nm下甘草酸标准曲线绘制
绘制标准曲线,如图1所示,可得标准曲线的线性方程为Y=8E+6X-85671,相关系数:R2=0.9965。
通过静态吸附单因素试验结果表明,选用D101大孔吸附树脂作为填充材料分离纯化甘草酸,吸附性能最好,且洗脱容易,确定为分离纯化甘草酸的首选树脂。在静态吸附-解吸实验中得出如下:随着上样体积的增加,甘草酸的吸附率、解吸率、转化率呈减小趋势;随着解吸液体积的增加,甘草酸的吸附率差别不大,呈微弱的减小趋势,而解吸率和转化率均呈上升趋势;偏酸性的上样液利于甘草酸纯化;随着上样乙醇浓度的增加,大孔树脂D101对甘草酸的吸附率、解吸率、转化率基本呈减小趋势;随着解吸液乙醇浓度的增加,大孔树脂D101对甘草酸的吸附率、解吸率、转化率基本呈上升趋势;甘草酸的吸附率、转化率与吸附时间、解吸时间的关系不大。
3.2大孔吸附树脂动态吸附-解吸的单因素试验
结合大孔树脂静态吸附-解吸试验,设计动态吸附-解吸试验。通过动态吸附单因素试验设计结果表明,选用D101大孔吸附树脂作为填充材料分离纯化甘草酸,用20 %乙醇溶解粗品,上样浓度2 mg·ml-1,上样体积1 BV,上样液pH=5,解吸液为70 %乙醇,解吸液用量为5 BV,吸附时间为1.5 h,解吸附时间为2 h。综合以上筛选条件,试验结果如表2。
表2 综合优选实验条件
上样体积(BV) | 解吸液体积(BV) | 上样pH | 上样浓度(mg·ml-1) | 上样液乙醇液浓度(%) | 解吸液浓度(%) | 吸附时间(h) | 解吸时间(h) | 吸附率% | 解吸率% | 转化率% | 纯度% |
1 | 5 | 5 | 2 | 20 | 70 | 1.5 | 2 | 71.4 | 93.3 | 83.68 | 37.23 |
1 | 5 | 5 | 2 | 20 | 70 | 1.5 | 2 | 62.6 | 92.7 | 78.34 | 36.81 |
1 | 5 | 5 | 2 | 20 | 70 | 1.5 | 2 | 73.1 | 89.3 | 75.62 | 35.32 |
平均组 | | | | | | | | 69.03 | 91.76 | 79.21 | 36.45 |
4.结论
通过静态吸附-解吸附试验证实大孔树脂D101吸附率高、易解吸,具有较高的吸附性能和解吸率,适用于甘草酸的纯化研究。通过动态吸附-解吸附试验中进一步得到最佳分离纯化甘草酸的工艺条件:用20 %乙醇溶解粗品,上样浓度2 mg·ml-1,上样体积1 BV,上样液pH=5,解吸液为70 %乙醇,解吸液用量为5 BV,吸附时间为1.5 h,解吸附时间为2 h。在最佳单因素组合条件下,甘草酸的吸附率为69.03%,解吸率为91.76%,转化率为79.21%,纯度为36.45%。因不同的纯化方法各具优缺点,未来还需进一步研究与探索,使得甘草酸在工业生产中创造更大价值。
参考文献
[1] 王建国,周忠.甘草的活性成分及其在化妆品中的应用[J].日用化学工业,2004,34(4):249-251.
[2] 来庚,张军良,杨来顺,等.大孔树脂法精制甘草酸[J].应用化工, 2006,35(4): 316-318.
[3] 王金丹.甘草酸提取纯化工艺研究进展[J].本溪化学工业学校:农业科技与装备,2020,299(5):62-63.
[4] 孙啸涛,李奈,王昌涛.高效液相色谱法评价大孔树脂纯化甘草酸工艺[J].食品科学,2013,34(6):39-97.
[5] 刘应蛟,曾晓艳,赵昱博,等.乌拉尔甘草HPLC指纹图谱建立及甘草苷和甘草酸的含量测定[J].中国药师,2021,24(04):738-741.
[6] 李军,杨奇,刘立轩,李敏,等.甘草颗粒中甘草酸含量HPLC测定方法的建立[J].动物医学进展,2020,41(12):74-79.
[7]张浩.HPLC法测定甘草中甘草苷和甘草酸含量[J].临床医药文献电子杂志,2020,7(48):10.