1. 陕西国际商贸学院 医药学院 陕西 西安 712046
摘要:二茂铁作为一种结构特殊的金属有机化合物,具有特殊的理化性质及生物活性。二茂铁类化合物以其特殊的性质而被广泛的应用于生物医药、功能材料、电化学分析及有机手性催化剂的制备方面,并显示出了优异的应用前景。本文根据二茂铁类化合物的应用领域不同,对其应用进行综述,期望对二茂铁类化合物的研究及开发提供一定的参考。
关键词:二茂铁;二茂铁衍生物;应用;进展
1 手性方酰胺的结构特征
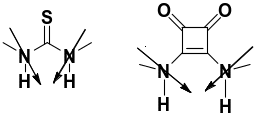
手性方酰胺主要有以下四个特征:第一个特征是表现出二元性,实验数据表明手性方酰胺在两部分键合当中很容易参与键合。一方面又因为手性方酰胺得结构包括两个氢键供体(N-H)和两个羰基受体(C=O),所以使得手性方酰胺具有双功能氢键功能。手性方酰胺还能形成一种第三方的氢键性质以及自身的二聚物,具有受电子性和供电子的性质(图1所示)。
第二个特征是具有刚性结构,研究发现在手性方酰胺催化剂的结构中,氨基的氮原子连接在烯键上,含有环四丁烯二酮,氨基的N原子跟烯间上面的C共存一个平面,很大程度上限制了方酰胺结构上N、C所形成的单键旋转,所以表明手性方酰胺具有刚性结构。
第三个特征是我们在手性方酰胺的晶体研究中发现,手性方酰胺上N键上的H之间的距离约为2.72Å,硫脲上的H之间距离为约为2.13Å。我们确定手性方酰胺双氢键的距离与硫脲催化剂上双氢间的距离约为0.6 Å。
第四个特征是是由于手性方酰胺的双氢键上距离与硫脲上的双氢的距离约为0.6Å,所以手性方酰胺的结构能诱导其的氮氢键向内收敛(如图2所示)。
2 手性方酰胺在不对称催化中的应用
2.1不对称醛酮还原
手性方酰胺作为一种新型的催化剂,其应用于不对称催化领域最早报道于四川大学谢如刚课题组。经过对催化剂的筛选,发现方酰胺催化剂表现出优异的活性以及选择性,此项突破性的探索发现受到不对称催化领域研究者的青睐(如图3所示)。
周海兵课题组首先用l,2-二苯基-2-氨基乙醇高产率地合成了一系列含有胺基、烷氧基及烷硫基的手性配体。用该类配体来催化溴代苯乙酮的不对称还原反应的实验结果数据。实验表明反应得到的手性仲醇的化学产率约在85-100%之间。而且该课题组对反应条件进行优化对比处理,实验发现其在甲苯中反应比在CH2Cl2或THF中可得到更高的对映体超量,反应温度最适宜为50℃,温度升高或降低均会影响对映体超量,配体最适宜的当量数为0.1当量(如图4所示)。
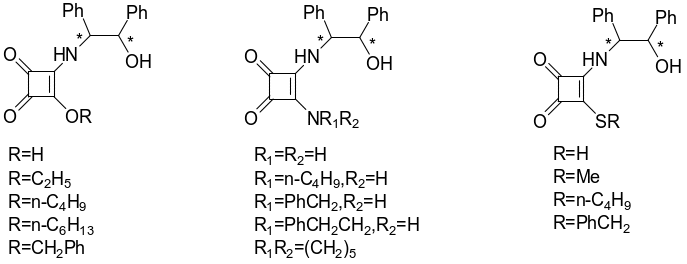
对于单酮来讲,当配体的当量数减至0.05时,对映体超量超过单手性中心配体催化的反应。就以前手性二酮而言,反应手性配体能获得极高的对映体超量,所以目标化合物的结构随着氨基醇结构的变化而改变(如图5)。
2.2不对称迈克加成反应
2009年,化学领域研究组Rawal在不对称反应中,经合成研究发现了一种具有金鸡钠碱衍生物性质的手性方酰胺双功能催化剂。该研究组以CH2Cl2溶剂,少量的该催化剂,在加成反应中成功发生了催化反应,所得目标化合物的含量极高(图6)。
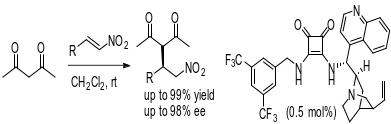
2011年,含有金鸡钠碱衍生物的一种手性方酰胺催化剂被杜大明教授合成出。在一定为温度,二氯为反应溶剂的情况下,查尔酮跟硝基甲烷发生不对称迈克加成反应。杜大明采用两种不同结构的金鸡钠碱手性方酰胺催化剂,所得目标化合物的含量极高(图7)。

同年,杜大明教授在研究的基础上合成了一种方酰胺催化剂,用三氟甲基取代了含金鸡纳碱衍生物,以CH2Cl2 为溶剂,在丙二腈和查尔酮的迈克加成反应中,发生较好的催化效果,所得目标化合物的含量极高(图8)。
2011年,在反应研究中催化硫醇与查尔酮的不对称迈克加成反应中,陈芬儿教授课题组在Rawal合成一种催化剂。在25℃温度下,甲苯和该催化剂的一定的催化剂量发生反应后,所得目标化合物的含量很高(图9)。
图9
2011年许丹倩教授等人合成了 1,2-二苯基乙二胺衍生的手性方酰胺催化剂。反应温度为25℃,以CHCl3为溶剂,发生不对称迈克加成反应,发现光学纯度很高,获得了较高的对映体超量(如图12所示)。
2.3不对称Friedel-Ctafts烷基化反应
2010年,Rawal等报道了一种方酰胺催化剂。在一定温度下,四氢呋喃为溶剂,一定剂量的该催化剂,在三氟丙酮酸酯与吲哚衍生物的不对称Friedel-Ctafts烷基化反应作用,获得了较高的对映体超量(图11)。

2012年,周海兵教授课题组合成了一种新型的催化剂。四氢呋喃为溶剂,室温条件下,一定剂量的该催化剂,在吲哚类化合物与苯磺酰亚胺类化合物不对称Friedel-Ctafts烷基化反应中,发现光学纯度很高,获得了较高的对映体超量(图12)。
2.4手性方酰胺催化的其他反应
2012年,彭云贵等合成了一种具有新型结构的手性方酰胺催化剂。在anlti-Mauwnich不对称反应中,溶剂为1,2-二氯乙烷,一定的温度下,一定剂量的该催化剂,反应一定时间,实验获得较高的对映体超量(图13)。

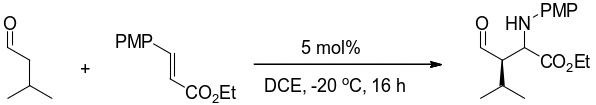
3结论
手性方酰胺作为一类结构特殊的手性催化剂,具有良好的氢键供体催化活性及选择性。综述前人的研究成果及进展,能够有效地指导研究者们根据手性方酰胺的特殊结构和有机物手性小分子的优点,设计合成出更多新颖结构的手性方酰胺催化剂,并期望能够在不对称催化反应中取得较高的对映选择性和较高的收率。
参考文献
[1]刘斌. 新型手性方酰胺催化剂的设计合成及其在不对称催化反应中的应用[D]. 武汉:武汉大学, 2014.
[2]戴乐.双功能手性方酰胺催化剂促进的不对称硫代Michael加成反应研究[D].上海:复旦大学, 2011.
[3]何海晓. 方酰胺催化杂环亚胺的不对称反应研究[D]. 北京:北京理工大学, 2015.
[4]刘建波. 手性方酰胺催化的不对称Michael加成反应研究[D]. 武汉:武汉理工大学, 2014.
基金项目:2021年陕西省大学生创新创业训练计划项项目“手性方酰胺催化剂的合成及其在不对称催化反应中的应用”(S202113123043)。.
作者简介:白文辉(1997-),男,药学专业,本科生在读。
*通讯联系人:高艳蓉(1989-),女,硕士,讲师,研究方向:有机合成。