天津医科大学第一中心临床学院(天津300000);2.天津市第一中心医院
(天津300000);3.天津市武清区第二人民医院(天津301700)
【摘要】目的:观察艾曲波帕在免疫相关性全血细胞减少症患者治疗中的疗效和副作用。方法:①35例明确诊断的免疫相关性全血细胞减少症患者接受艾曲波帕治疗;②患者接受原治疗基础上,接受艾曲波帕治疗25mg·d1口服,其后每7天依据血常规计数评价疗效,无效者提高艾曲波帕剂量为:50~100mg·d1口服;③血常规达到完全缓解,继续原剂量或降低剂量,减量过程中,如血细胞再度下降,提高到减量前的原剂量;④患者出现严重副作用、脏器功能损害不能耐受,停用艾曲波帕治疗并退出临床观察;⑤观察治疗期间达到完全缓解的例数及减量后血常规变化。结果:①15例(48.39%)患者白细胞水平达到CR,患者达到CR的中位时间为28天。16例(51.61%)患者血红蛋白水平达到CR,患者达到CR的中位时间为35天。25例(80.65%)患者血小板水平达到有效、18例(58.06%)患者达到CR,患者达到CR的中位时间为19天;②11例(35.48%)患者三系均达到CR,中位时间为29天;③三系分别达到CR的比例,差异无统计学意义;④艾曲波帕治疗减量,9例患者0.5~2月后,血小板及白细胞水平再度降低,恢复之前剂量继续治疗,8/9例患者恢复造血。⑤艾曲波帕治疗,副作用可以耐受。结论:艾曲波帕治疗免疫相关性全血细胞减少症,三系达到CR的百分比差异无统计学意义;且耐受性良好。
【关键词】艾曲波帕;免疫相关性;全血细胞减少症;疗效
【Abstract】Objective To observe the efficacy and side effects of Eltrombopag in the treatment of immune related pancytopenia. Methods Thirty-five patients with immune related pancytopenia received Eltrombopag therapy. On the basis of the original treatment, the patients were treated with Eltrombopag of 25~100mg every day. If the blood routine achieved complete remission (CR), Eltrombopag treatment could reduce the amount. The patient suffered from severe side effects and organ dysfunction, so the Eltrombopag treatment was stopped and the clinical observation was withdrawn. Results ①15 patients (48.39%) had a white blood cell level of CR, the median time to CR was 28 days. 16 patients (51.61%) had a hemoglobin level of CR, the median time to CR was 35 days. 25 patients (80.65%) had a effective platelet levels, and 18 patients (58.06%) reached CR. The median time to CR of platelet was 19 days. ② CR was achieved in all the three blood cells in 11 patients (35.48%), the median time to CR was 29 days. ③The proportions of CR in all the three blood cells were not statistically significant.④After the CR was achieved, the platelet and white blood cell levels of 9 patients were reduced again after 0.5~2 months of reduction of Eltrombopag dose. The hemocytopenia was restored in 8/9 patients after the previous Eltrombopag dose was resumed. ⑤The side effects of Eltrombopag therapy could be tolerated. Conclusion In the treatment of immune related pancytopenia, there was no statistically significant difference in the percentage of CR among the three blood cells, while the side effects of Eltrombopag could be tolerated.
【Key words】Eltrombopag;Immune correlation;Pancytopenia;curative effect;side effects
艾曲波帕是一种促血小板生成素受体激动剂,是第一个口服治疗ITP的药物,为非肽类小分子受体激活剂,结合于骨髓巨核细胞上重组人血小板生成素(Recombinant Human Thrombopoietin, TPO)受体(c-Mpl)的跨膜区,引起细胞质的酪氨酸激酶Janus 2(JAK2)和酪氨酸激酶(Tyrosine kinase,Tyk)2的活化,信号转导及转录激活因子(Signal transducer and activator of transcription,STAT)-5、丝裂原活化蛋白激酶(Mitogen-activated protein kinase,MAPK)、细胞外信号调节激酶(Extracellular regulated kinase,ERK)1/2等信号通路相关因子的磷酸化,诱导聚合细胞从骨髓祖细胞的增值和分化,刺激血小板生成。免疫相关性全血细胞减少症,临床主要表现为贫血、出血、感染;血常规呈三系、二系或一系血细胞减少,而网织红细胞百分比不低,骨髓增生活跃或明显活跃。在此,我们观察了艾曲波帕在免疫相关性全血细胞减少症患者的治疗中,白细胞、血红蛋白以及血小板恢复的情况,及其副作用。
1.病例和方法
1.1 病例:本研究回顾性分析35例免疫相关性全血细胞减少症患者接受艾曲波帕治疗的疗效和副作用。收集2018年1月至2019年12月在我院住院及门诊确诊的免疫相关性全血细胞减少症患者的临床资料,包括性别、年龄、入组时免疫指标、血常规指标、诊断距接受本研究的时间间隔、入组之前治疗情况、并发症情况等。
1.2实验室检查:①血、尿常规、网织红细胞计数、肝肾功能、铁蛋白、肝炎指标检测;②溶血检测:凝集实验法进行抗人球蛋白试验检测、流式细胞法检测CD55和CD59表达;③免疫学检查:胶乳凝集试验法检测类风湿因子、间接免疫荧光法检测抗核抗体、免疫比浊法检测免疫球蛋白、放射免疫分析法检测甲状腺抗体;④骨髓形态及染色体核型分析;⑤肝、脾影像学检查。
1.3治疗方法:所有患者原治疗方案维持条件下,且肝功能等脏器功能正常,接受艾曲波帕治疗,剂量为:25mg·d1口服,其后每7天依据血常规计数评价疗效,无效者提高艾曲波帕剂量为:50-100mg·d1口服。每7天血常规计数评价疗效、每14天肝肾功能等检测观察副作用(其中肝移植后4例患者每周复查肝功能)。待血细胞计数提高、病情稳定,延长监测周期为每月一次血常规和肝肾功能检测。血常规达到白细胞:4.0×109/L,血色素:120g/L,血小板:100×109/L以上,继续原剂量维持或降低剂量25mg·d1的用药剂量。减量过程中,如血细胞再度下降,提高到减量前的原剂量继续治疗。
1.4临床观察退出标准:患者接受艾曲波帕治疗期间,出现严重副作用、脏器功能损害不能耐受继续治疗者,即刻停用艾曲波帕治疗,退出临床观察。
1.5疗效评价:疗效评估方法,每周定期监测全血细胞计数,包括白细胞(WBC)计数、血红蛋白(Hb)水平、血小板(Plt)计数。WBC>4.0×109/L且中性粒细胞>2.0×109/L为完全缓解(Complete response,CR)。Hb>120g/L(>110g/L,女)为CR。Plt>100×109/L为CR;Plt>30×109/L且比基础Plt增加2倍并无出血为有效;Plt<30×109/L且比基础Plt增加不到2倍并有出血为无效。初次疗效评价时间为艾曲波帕治疗后1个月进行血常规检测,患者每个月接受疗效评价,直至本研究的观察时间终点2020年6月,所有患者至少观察6个月时间。本研究35例患者4例失访,参加疗效评价患者31例。
1.6统计学处理:统计学处理采用SPSS17.0进行。患者血常规WBC、Hb、Plt 达到CR的比例,组间比较采用卡方检验,P<0.05为差异具有统计学意义。
2.结果
2.1一般资料:除外失访患者,本研究中患者共31例,男9例,女22例,中位年龄为43.8(11-75)岁,临床资料见表1。所有患者均经检查明确诊断为免疫相关性全血细胞减少症,至少存在包括血小板减少在内的另外一系血小板减少、且均为至少接受糖皮质激素治疗大于1个月,且无效患者。其中,包括7例肾移植术后、4例肝移植术后患者,因血细胞减少诊断为免疫相关性全血细胞减少症。
表1 患者基线特征
临床特征 | 患者情况,n(%)(N=31) |
年 龄 (岁) 性 别 男 女 诊断据本研究时间均值 (月) 血细胞减少情况 二系减少 三系减少 入组前接受治疗线数 1 2 3 入组前接受治疗种类 糖皮质激素 免疫抑制剂 利妥昔单抗 两个及以上联合治疗 | 43.8(11~75) 9(29.03) 22(70.97) 8.3(月) 31(100) 24(77.42) 31(100) 22(70.97) 14(45.16) 31(100) 18(58.06) 7(22.58) 19(61.29) |
2.2患者排除情况:所有患者接受艾曲波帕治疗期间,副作用轻微、患者各项临床指标监测,不影响继续治疗,无因副作用而排除的病例。
2.3血细胞水平恢复情况:
(1)白细胞计数:1个月初次评价疗效,31例患者中有5例(16.13%)CR;2个月评价9例(29.03%)患者CR;3个月评价15例(48.39%)患者CR;4个月后患者疗效评价无变化(图1A)。患者白细胞水平达到CR的中位时间为28天[95% CI,7~95天]。
(2)血色素水平:1个月初次评价疗效,31例患者中无CR ;2个评价疗效5例(16.13%)患者CR;3个月评价8例(25.81%)患者CR;4个月评价15例(48.39%)患者CR;5个月评价16例(51.61%)患者CR;6个月后患者疗效评价无变化(图1A)。患者血色素水平达到CR的中位时间为35天[95% CI,21-121天]。
(3)血小板计数:1个月初次评价疗效,31例患者中12例(38.71%)有效,4例(12.90%)患者CR;2个月评价疗效,17例(54.84%)患者有效,12例(38.71%)患者CR;3个月评价,25例(80.65%)患者有效,18例(58.06%)患者CR;4个月后患者疗效评价无变化(图1A)。患者血小板水平达到CR的中位时间为19天[95% CI,7-28天]。
(4)三系水平观察:1个月初次评价疗效,无CR患者;2个月评价疗效,3例(9.68%)患者CR ;3个月评价,6例(19.36%)患者CR;4个月评价,10例(32.26%)患者CR;5个月评价,11例(35.48%)患者CR;6个月后患者疗效评价无变化(图1 B)。患者三系达到CR的中位时间为29天[95% CI,28-121天]。
(5)三系分别达到CR比例的统计学差异:本研究观察时间内,WBC共15例(48.39%)达到CR;Hb共16例(51.61%)达到CR;Plt共18例(58.06%)达到CR。达到CR的比例,WBC与Hb比较,差异无统计学意义(P=1.817);WBC与Plt比较,差异无统计学意义(P=1.513);Hb与Plt比较,差异无统计学意义(P=2.999)。
2.4远期疗效和药物减量的疗效评价:2个月初次评价疗效后,25例患者血小板或三系达到CR后,艾曲波帕治疗减量(未停药)。其中9例患者减量后于0.5~2月,血小板水平再度降低,其中4例合并白细胞下降,无血色素水平降低。9例患者艾曲波帕治疗均恢复之前剂量继续治疗。其中8例患者恢复剂量后1-2月血小板水平逐渐恢复CR,另外1例患者观察4月余血小板未得到恢复。9例患者恢复剂量后1-2月白细胞水平均恢复CR(图2)。
2.5副作用观察:患者治疗过程中,观察其副作用,出现乏力、皮疹、头痛、食欲减低、腹泻等副作用(表2),对症支持治疗可缓解、或自愈。大部分副作用出现在服药起始阶段,即服药1个月内。本研究观察时间比较短,未出现严重的安全事件包括白内障、血栓栓塞事件、骨髓纤维化,仅4例患者出现肝功能损害及胆红素增高,见表2。
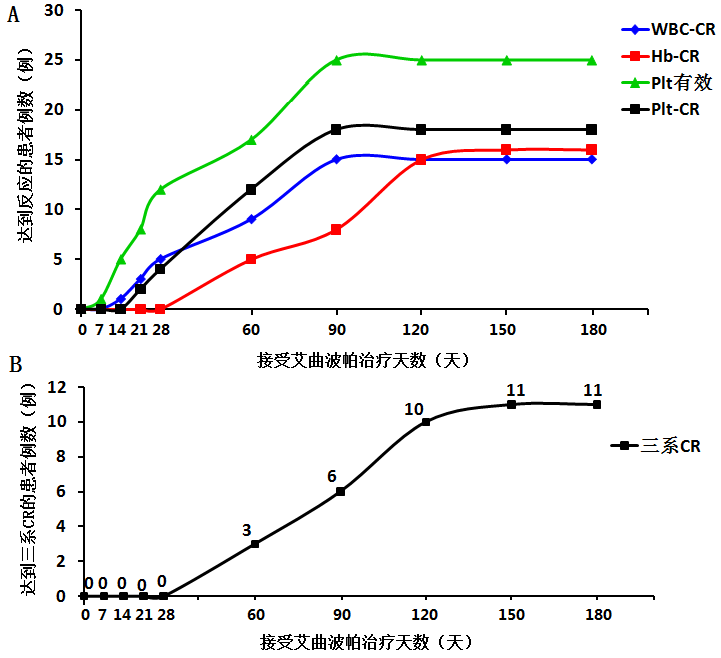
图1 艾曲波帕治疗疗效分析
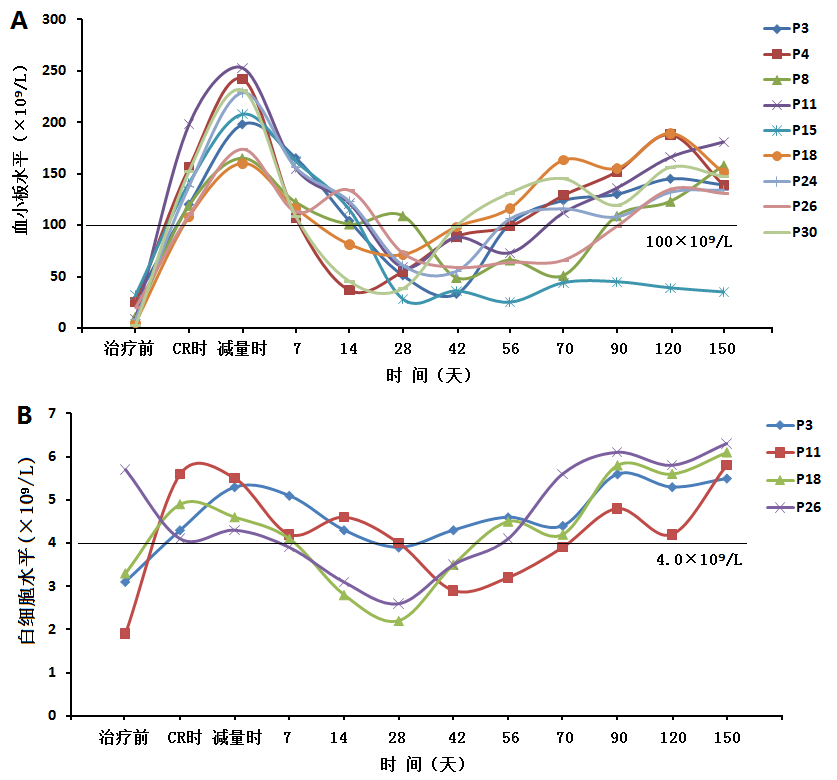
图2 艾曲波帕减量后血细胞水平变化
表2 艾曲波帕治疗副作用
副作用 | 例数(%)(N=31) |
全部副作用 头痛 乏力 皮疹 恶心 腹泻 食欲减低 咳嗽 关节痛 严重副作用 白内障 肺炎 转氨酶增高 胆红素增高 深部静脉血栓 | 19(61.29) 4(12.9) 6(19.35) 5(16.13) 3(9.68) 2(6.45) 1(3.23) 2(6.45) 4(12.9) 4(12.9) 0(0) 0(0) 3(9.68) 1(3.23) 0(0) |
3.讨论
免疫相关性全血细胞减少症(Immune related pancytopenia,IRP)是由多种原因引起的T淋巴细胞调控失衡导致B淋巴细胞功能亢进产生抗造血细胞自身抗体,破坏或抑制骨髓造血所致的一种血细胞减少性疾病。其临床表现为:(1)全血细胞减少,网织红细胞和中性粒细胞比例高或正常;(2)骨髓有核红细胞比例正常或增高,显微镜下常可见“红细胞岛”;(3)已知的血液病,包括再生障碍性贫血(AA)。IRP存在复杂的免疫调节失衡,除了纠正贫血 、控制出血和感染、维护重要脏器功能等一些对症治疗外,多采用非细胞毒免疫抑制剂治疗、细胞毒免疫抑制剂治疗和造血干细胞移植。艾曲波帕通过与c-MPL 跨膜结构域结合以激活下游JAK/STAT信号转导通路,促进多系造血。 本研究选择了此类疾病,均为至少经过糖皮质激素治疗无效患者,观察艾曲波帕治疗的疗效,特别是针对白细胞和血红蛋白减少的疗效。
艾曲泊帕是一种小分子非肽类的口服血小板生成素受体激动剂(TPO-RA),它与TPO-R的跨膜域结合,诱导巨核细胞系中骨髓(BM)祖细胞的增殖和分化,能在造血干细胞水平刺激血小板的产生,因此艾曲泊帕为免疫性血小板减少症(ITP)患者提供了新的治疗途径。艾曲泊帕是治疗慢性ITP的有效药物,长期治疗患者耐受性良好,艾曲泊帕长期维持治疗能够使部分患者保持血小板计数稳定,维持临床疗效。但既往的临床试验结果显示,停止艾曲泊帕治疗后,大部分患者血小板计数下降,且停药后血小板下降有显著性意义。
艾曲波帕在多种疾病中已经有一定的应用经验,再生障碍性贫血(Aplastic anemia, AA)疗效有限,艾曲泊帕被批准用于复发性/难治AA患者。多项研究表明艾曲波帕对造血干细胞有刺激作用,且艾曲波帕的血液学反应具有药物剂量依赖性。Desmond等对IST无效的43例重症AA患者给予艾曲波帕治疗,其血液学应答率在40%,且能看到血液学多系反应。其中5例患者在随访28.5个月后达到血细胞计数恢复的标准,逐渐减少并停止使用艾曲波帕后仍未复发。另外,艾曲波帕在AA治疗中,免疫抑制剂联合应用6个月,总反应率为94%,其中达到CR。与前期应用艾曲波帕单药相比,CR率增加近1倍,且肝酶、克隆演变情况无明显升高[。骨髓增生异常综合征(Myelodysplastic syndrome,MDS)是多能造血干细胞的克隆性恶性肿瘤,其特征是造血无效导致细胞减少。血小板减少症发生在40-65%的MDS患者中,并预示着更差的预后。尽管艾曲泊帕未获批准用于MDS,但有报道该药物对超过三分之一的MDS患者有效。
本研究针对免疫相关性全血细胞减少症,至少经过糖皮质激素治疗失败患者,选择了艾曲波帕治疗。观察到良好的反应,特别是不仅针对血小板减少具有良好的反应,对白细胞和血红蛋白水平的提升也具有非常好的疗效。本组病例中的治疗反应率,达到CR的百分比,三系无统计学差异。另外,达到CR后减量艾曲波帕问题,部分患者复发,但剂量恢复后仅一例患者没有恢复造血,其余患者均恢复。因此,艾曲波帕可以用于难治免疫相关性全血细胞减少症的治疗,而且达到理想疗效后可以考虑艾曲波帕逐渐减量。
艾曲泊帕具有很好的耐受性,常见不良反应包括头痛、恶心、呕吐、血栓栓塞,还可引起丙氨酸氨基转移酶和胆红素升高,部分患者会出现骨髓网硬蛋白沉积、骨髓纤维化。本组患者安全性亦良好,所有31例患者无肝功能异常等严重不良反应出现。
【参考文献】
[1]孙慧平,范青叶等.艾曲泊帕长期治疗成人慢性免疫性血小板减少症的疗效和安全性[J].临床血液学杂志,2020,33(1):39-43.
[2]Gill H,Wong RSM, Kwong YL.From chronic immune thrombocytopenia to severe aplastic anemia: recent insights into the evolution of eltrombopag [J]. Ther Adv Hematol,2017,8(5):159-174.
[3]Gonzalez-Porras JR,Bastida JM. Eltrombopag in immune thrombocytopenia:efficacy review and update on drug safety[J].Ther Adv Drug Saf,2018,9(6):63.
[4]Scheinberg P.Recent advances and long-term results of medical treatment of acquired aplastic anemia:are patients cured[J]. Hematology/Oncology Clinics of North America,2018,32(4):609-618.
[5]Winkler T,Cooper JN,Townsley DM,et al.Eltrombopag for refractory severe aplastic anemia:dosing regimens, Long-term follow-up,clonal evolution and somatic mutation profiling[abstract].Blood, 2017,10(l1):777.
[6]Gill H,Leung GM,Lopes D,et al.The thrombopoiet in mimetics eltrombopag and romiplostim in the treatment of refractory aplastic anaemia[J].Br J Haematol,2017,16:991-994.
[7]Townsley DM,Scheinberg P,Winkler T,et al.Eltrombopag added to standard immunosuppression for aplastic anemia[J].N Engl J Med, 2017,36:1540-1550.
[8]Lindsley RC.Uncoding the genetic heterogeneity of myelodysplastic syndrome[J].Hematology Am Soc Hematol Educ Program, 2017,1:447-452.
[9]Swaminathan M,Borthakur G,Kadia TM,et al.A phase 2 clinical trial of eltrombopag for treatment of patients with myelodysplastic syndromes after hypomethylating-agent failure[J].Leuk Lymphoma, 2019,18:1-7.
【作者简介】李征(1988.10-),女,汉族,天津市人,天津市武清区第二人民医院内科主治医师,天津医科大学血液病学在职硕士研究生,主要研究方向:内科常见疾病的诊断和治疗。
【通讯作者】邓琦(1972.03-),女,汉族,广东省江门市人,硕士研究生学历,天津市第一中心医院血液科主任医师,主要研究方向:血液病与细胞免疫治疗。